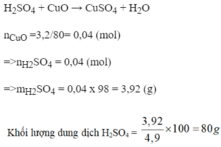cho 3,2g cuo tác dụng vừa đủ với dung dịch h2so4 4,9% thu được muối cuso4 và nước. tính nồng độ % của dung dịch cuso tạo thành

Những câu hỏi liên quan
cho 4 g CuO tác dụng vừa đủ với dung dịch H2SO4 4,9% thu được muối CuSO4 và H2O
a, Tính khối lượng dung dịch H2SO4 cần dùng
b, Tính nồng đọ phần trăm dung dịch CuSO4 sau phản ứng tạo thành
giúp mình với các bạn ơi . Thank you
Câu 9. Cho 3,2g CuO tác dụng vừa đủ với dung dịch H2SO4 4,9%
a)Viết PTHH
b) Tính nồng độ % của dung dịch CuSO4 (Biết Cu =64; H=1; S=32; O=16)
:3
Cho 3.2g CuO tác dụng vừa đủ với dung dịch H2SO4 4.9% thu được CuSO4 và nước. Tính nồng độ % của dung dịch CuSO4 tạo thành.
Các tiền bối giúp đỡ ạ!
\(n_{CuO}=\dfrac{3,2}{80}=0,04\left(mol\right)\\
pthh:CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
0,04 0,04 0,04 0,04
\(m_{\text{dd}_{H_2SO_4}}=\dfrac{\left(0,04.36,5\right).100}{4,9}=29,79\left(g\right)\\
m_{\text{dd}_{CuSO_4}}=3,2+29,79-\left(0,04.2\right)=32,91\left(g\right)\\
C\%_{\text{dd}}=\dfrac{0,04.160}{32,91}.100\%=19,44\%\)
Đúng 2
Bình luận (0)
cho 3,2 g cuo tác dụng vừa đủ với dung dịch H2SO4 , 4,9%. Tính nồng độ phần trăm của dung dịch CuSO4
nCuO=0,04 mol
CuO + H2SO4 =>CuSO4 + H2O
0,04 mol=>0,04 mol=>0,04 mol
mH2SO4=0,04.98=3,92 gam
=>m dd H2SO4=3,92/4,9%=80 gam
mCuSO4 sau=0,04.160=6,4 gam
mdd CuSO4=3,2+80=83,2 gam
C% dd CuSO4=6,4/83,2.100%=7,69%
Đúng 0
Bình luận (0)
cho \(m_{CuO}=3,2g\Rightarrow n_{CuO}=\frac{3,2}{80}=0,04mol\)
PTHH:
CuO + H2SO4 -> CuSO4 + H2O
0,04mol----------->0,04mol--------->0,04mol
ta có: \(m_{H_2SO_4}=0,04.98=3,92g\)
\(C\%_{d^2H_2SO_{4_{ }}}=4,9\%\)
=. \(m_{d^2H_2SO_4}=\frac{m_{H_2SO_4}.100}{C\%}=\frac{3,92.100}{4,9}=80g\)
áp dụng ĐLBTKL ta có: \(m_{d^2CUSO_4}=m_{CuO}+m_{d^2H_2SO_4}=3,2+80=83,2g\)
\(m_{CuSO_4}=0,04.160=6,4g\)
\(\Rightarrow C\%_{d^2CuSO_4}=\frac{m_{CuSO_4}}{m_{d^2CuSO_4}}.100=\frac{6,4}{83,2}.100=7,69\%\)
Đúng 0
Bình luận (0)
Cho 3,2 gam CuO tác dụng vừa đủ với dung dịch H 2 S O 4 4,9%. Tính nồng độ % của dung dịch CuSO4 (Cu = 64, H = 1, S = 32, O = 16).
Cho 3,2gam \(CuO\) tác dụng vừa đủ với dung dịch \(H_2SO_4\) 4,9%
a. Viết PTHH
b. Tính nồng độ % của dung dịch CuSo4 10%
a) \(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
b) \(n_{CuO}=\dfrac{3,2}{80}=0,04\left(mol\right)=n_{H_2SO_4}=n_{CuSO_4}\)
\(m_{ddH_2SO_4}=\dfrac{0,04.98}{4,9\%}=80\%\)
\(m_{ddsaupu}=3,2+80=83,2\left(g\right)\)
=> \(C\%_{CuSO_4}=\dfrac{0,04.160}{83,2}.100=7,69\%\)
Đúng 2
Bình luận (0)
dạ đây là toán 9 ạ mong anh chị thầy cô giúp đỡ em ạ .BT1: Cho 3,2g Đồng oxit ta1xc dụng vừa đủ với dung dịch H2SO4 , 4,9% .Tính nồng độ phần trăm của dung dịch CuSO4BT2 : Biết rằng 1,12l khí cacbon đioxit (điều kiện tiêu chuẩn) tác dụng vừa đủ với 100 ml dung dịch NaOH tạo ra muối trung hòa a) Viết chương trình hóa học b) Tính nồng độ mol của dung dịch NaOH đã dùng dạ 2 bài tập quá nhiều nhưng em cần rất gấp mong anh chị thầy cô giúp đỡ em ạ . Em xin chân thành cảm ơn.
Đọc tiếp
dạ đây là toán 9 ạ mong anh chị thầy cô giúp đỡ em ạ .
BT1: Cho 3,2g Đồng oxit ta1xc dụng vừa đủ với dung dịch H2SO4 , 4,9% .Tính nồng độ phần trăm của dung dịch CuSO4
BT2 : Biết rằng 1,12l khí cacbon đioxit (điều kiện tiêu chuẩn) tác dụng vừa đủ với 100 ml dung dịch NaOH tạo ra muối trung hòa
a) Viết chương trình hóa học
b) Tính nồng độ mol của dung dịch NaOH đã dùng
dạ 2 bài tập quá nhiều nhưng em cần rất gấp mong anh chị thầy cô giúp đỡ em ạ . Em xin chân thành cảm ơn.
Bài 1 chị giải ở trên rồi nhé em
Bài 2
nCO2=1,12/22,4=0,05 mol
CO2 +2 NaOH => Na2CO3 + H2O
0,05 mol=>0,1 mol
CM dd NaOH=0,1/0,1=1M
Đúng 0
Bình luận (0)
Bài 1. Cho 8 gam Copper (II) oxide (CuO) tác dụng vừa đủ với 200 mL dung dịch Hydrochloric acid (HCI). a) Tính khối lượng muối tạo thành. b) Tính nồng độ mol dung dịch Hydrochloric acid (HCI) đã dùng. c) Tính nồng độ mol dung dịch muối thu được. Biết sau phản ứng thể tích dung dịch thay đổi không đáng kể
\(a)n_{CuO}=\dfrac{8}{80}=0,1mol\\ CuO+2HCl\rightarrow CuCl_2+H_2O\\ n_{CuCl_2}=n_{Cu}=0,1mol\\ m_{CuCl_2}=0,1.135=13,5g\\ b)n_{HCl}=0,1.2=0,2mol\\ C_{M_{HCl}}=\dfrac{0,2}{0,2}=1M\\ c)C_{M_{CuCl_2}}=\dfrac{0,1}{0,2}=0,5M\)
Đúng 3
Bình luận (0)
Cho 4g CuO tác dụng vừa đủ với dung dịch H2SO4 loãng 0,5M
a. Viết phương trình hóa học
b. Tính khối lượng muối tạo thành
c. Tính thể tích dung dịch H2SO4 đã dùng
d. Tính nồng độ mol của muối có trong dung dịch sau phản ứng ( coi thể tích dung dịch không đáng kể )
\(n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\\a, CuO+H_2SO_4\rightarrow CuSO_4+H_2O\\ n_{CuSO_4}=n_{H_2SO_4}=n_{CuO}=0,05\left(MOL\right)\\ b,m_{CuSO_4}=0,05.160=8\left(g\right)\\ c,V_{ddH_2SO_4}=\dfrac{0,05}{0,5}=0,1\left(l\right)\\ d,V_{ddCuSO_4}=V_{ddH_2SO_4}=0,1\left(l\right)\\ C_{MddCuSO_4}=\dfrac{0,05}{0,1}=0,5\left(M\right)\)
Đúng 2
Bình luận (0)